Лечение суставов - артроз, артрит, остеохондроз и многое другое
Характерные признаки миелотоксического агранулоцитоза
Агранулоцитоз
Агранулоцитоз – клинико-гематологический синдром, в основе которого лежит резкое уменьшение или отсутствие нейтрофильных гранулоцитов среди клеточных элементов периферической крови. Агранулоцитоз сопровождается развитием инфекционных процессов, ангины, язвенного стоматита, пневмонии, геморрагических проявлений. Из осложнений часты сепсис, гепатит, медиастинит, перитонит. Первостепенное значение для диагностики агранулоцитоза имеет исследование гемограммы, пунктата костного мозга, обнаружение антинейтрофильных антител. Лечение направлено на устранение причин, вызвавших агранулоцитоз, предупреждение осложнений и восстановление кроветворения.
Агранулоцитоз – изменение картины периферической крови, развивающееся при ряде самостоятельных заболеваний и характеризующееся снижением количества или исчезновением гранулоцитов. В гематологии под агранулоцитозом подразумевается уменьшение количества гранулоцитов в крови менее 0,75х109/л или общего числа лейкоцитов ниже 1х109/л. Врожденный агранулоцитоз встречается крайне редко; приобретенное состояние диагностируется с частотой 1 случай на 1200 человек. Женщины страдают агранулоцитозом в 2-3 раза чаще мужчин; обычно синдром выявляется в возрасте старше 40 лет. В настоящее время в связи с широким использованием в лечебной практике цитотоксической терапии, а также появлением большого количества новых фармакологических средств частота случаев агранулоцитоза значительно увеличилась.
Агранулоцитоз
В первую очередь, агранулоцитозы подразделяются на врожденные и приобретенные. Последние могут являться самостоятельным патологическим состоянием или одним из проявлений другого синдрома. По ведущему патогенетическому фактору различают миелотоксический, иммунный гаптеновый и аутоиммунный агранулоцитоз. Также выделяют идиопатическую (генуинную) форму с неустановленной этиологией.
По особенностям клинического течения дифференцируют острые и рецидивирующие (хронические) агранулоцитозы. Тяжесть течения агранулоцитоза зависит от количества гранулоцитов в крови и может быть легкой (при уровне гранулоцитов 1,0–0,5х109/л), средней (при уровне менее 0,5х109/л) или тяжелой (при полном отсутствии гранулоцитов в крови).
Роль гранулоцитов в организме
Гранулоцитами называются лейкоциты, в цитоплазме которых при окрашивании определяется специфическая зернистость (гранулы). Гранулоциты вырабатываются в костном мозге, поэтому относятся к клеткам миелоидного ряда. Они составляют самую многочисленную группу лейкоцитов. В зависимости от особенностей окрашивания гранул эти клетки подразделяются на нейтрофилы, эозинофилы и базофилы – они различаются по своим функциям в организме.
На долю нейтрофильных гранулоцитов приходится до 50-75% всех белых кровяных телец. Среди них различают зрелые сегментоядерные (в норме 45-70%) и незрелые палочкоядерные нейтрофилы (в норме 1-6%). Состояние, характеризующееся повышением содержания нейтрофилов, носит название нейтрофилии; в случае понижения количества нейтрофилов говорят о нейтропении (гранулоцитопении), а в случае отсутствия – об агранулоцитозе. В организме нейтрофильные гранулоциты выполняют роль главного защитного фактора от инфекций (главным образом, микробных и грибковых). При внедрении инфекционного агента нейтрофилы мигрируют через стенку капилляров и устремляются в ткани к очагу инфекции, фагоцитируют и разрушают бактерии своими ферментами, активно формируя местный воспалительный ответ. При агранулоцитозе реакция организма на внедрение инфекционного возбудителя оказывается неэффективной, что может сопровождаться развитием фатальных септических осложнений.
Миелотоксический агранулоцитоз возникает вследствие подавления продукции клеток-предшественников миелопоэза в костном мозге. Одновременно в крови отмечается снижение уровня лимфоцитов, ретикулоцитов, тромбоцитов. Данный вид агранулоцитоза может развиваться при воздействии на организм ионизирующего излучения, цитостатических препаратов и других фармакологических средств (левомицетина, стрептомицина, гентамицина, пенициллина, колхицина, аминазина) и др.
Иммунный агранулоцитоз связан с образованием в организме антител, действие которых обращено против собственных лейкоцитов. Возникновение гаптенового иммунного агранулоцитоза провоцирует прием сульфаниламидов, НПВС-производных пиразолона (амидопирина, анальгина, аспирина, бутадиона), препаратов для терапии туберкулеза, сахарного диабета, гельминтозов, которые выступают в роли гаптенов. Они способны образовывать комплексные соединения с белками крови или оболочками лейкоцитов, становясь антигенами, по отношению к которым организм начинает продуцировать антитела. Последние фиксируются на поверхности белых кровяных телец, вызывая их гибель.
В основе аутоиммунного агранулоцитоза лежит патологическая реакция иммунной системы, сопровождающаяся образованием антинейтрофильных антител. Такая разновидность агранулоцитоза встречается при аутоиммунном тиреоидите, ревматоидном артрите, системной красной волчанке и других коллагенозах. Агранулоцитоз, развивающийся при некоторых инфекционных заболеваниях (гриппе, инфекционном мононуклеозе, малярии, желтой лихорадке, брюшном тифе, вирусном гепатите, полиомиелите и др.) также имеет иммунный характер. Выраженная нейтропения может сигнализировать о хроническом лимфолейкозе, апластической анемии, синдроме Фелти, а также протекать параллельно с тромбоцитопенией или гемолитической анемией. Врожденный агранулоцитоз является следствием генетических нарушений.
Патологические реакции, сопровождающие течение агранулоцитоза, в большинстве случаев представлены язвенно-некротическими изменениями кожи, слизистой оболочки полости рта и глотки, реже - конъюнктивальной полости, гортани, желудка. Некротические язвы могут возникать в слизистой кишечника, вызывая перфорацию кишечной стенки, развитие кишечных кровотечений; в стенке мочевого пузыря и влагалища. При микроскопии участков некроза обнаруживается отсутствие нейтрофильных гранулоцитов.
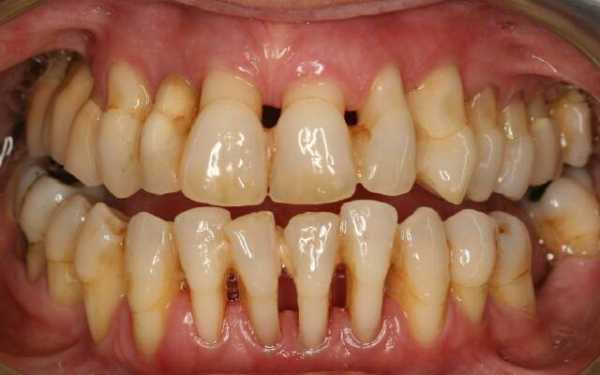
Клиника иммунного агранулоцитоза обычно развивается остро, в отличие от миелотоксического и аутоиммунного вариантов, при которых патологические симптомы возникают и прогрессируют постепенно. К ранними манифестным проявлениям агранулоцитоза относятся лихорадка (39-40°С), резкая слабость, бледность, потливость, артралгии. Характерны язвенно-некротический процессы слизистой оболочки рта и глотки (гингивиты, стоматиты, фарингиты, ангины), некротизация язычка, мягкого и твердого нёба. Данные изменения сопровождаются саливацией, болью в горле, дисфагией, спазмом жевательной мускулатуры. Отмечается регионарный лимфаденит, умеренное увеличение печени и селезенки.
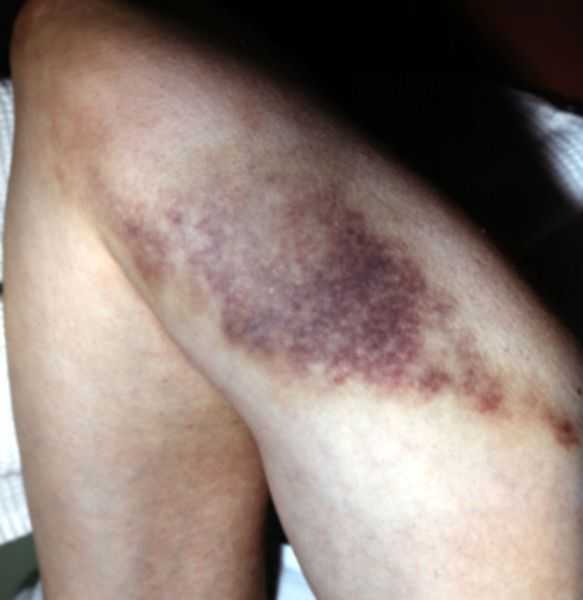
Для миелотоксического агранулоцитоза типично возникновение умеренно выраженного геморрагического синдрома, проявляющегося кровоточивостью десен, носовыми кровотечениями, образованием синяков и гематом, гематурией. При поражении кишечника развивается некротическая энтеропатия, проявлениями которой служат схваткообразные боли в животе, диарея, вздутие живота. При тяжелой форме возможны осложнения в виде прободения кишечника, перитонита.
При агранулоцитозе у больных могут возникать геморрагические пневмонии, осложняющиеся абсцессами и гангреной легкого. При этом физикальные и рентгенологические данные бывают крайне скудными. Из числа наиболее частых осложнений возможны перфорация мягкого нёба, сепсис, медиастинит, острый гепатит.
Группу потенциального риска по развитию агранулоцитоза составляют пациенты, перенесшие тяжелое инфекционное заболевание, получающие лучевую, цитотоксическую или иную лекарственную терапию, страдающие коллагенозами. Из клинических данных диагностическое значение представляет сочетание гипертермии, язвенно-некротических поражений видимых слизистых и геморрагических проявлений.
Наиболее важным для подтверждения агранулоцитоза является исследование общего анализа крови и пункция костного мозга. Картина периферической крови характеризуется лейкопенией (1-2х109/л), гранулоцитопенией (менее 0,75х109/л) или агранулоцитозом, умеренной анемией, при тяжелых степенях – тромбоцитопенией. При исследовании миелограммы выявляется уменьшение количества миелокариоцитов, снижение числа и нарушение созревания клеток нейтрофильного ростка, наличие большого количества плазматических клеток и мегакариоцитов. Для подтверждения аутоиммунного характера агранулоцитоза производится определение антинейтрофильных антител.
Всем пациентам с агранулоцитозом показано проведение рентгенографии легких, повторные исследования крови на стерильность, исследование биохимического анализа крови, консультация стоматолога и отоларинголога. Дифференцировать агранулоцитоз необходимо от острого лейкоза, гипопластической анемии. Также необходимо исключение ВИЧ-статуса.
Пациенты с верифицированным агранулоцитозом должны быть госпитализированы в отделении гематологии. Больные помещаются в палату-изолятор с асептическими условиями, где проводится регулярное кварцевание, ограничивается посещение, медицинский персонал работает только в шапочках, масках и бахилах. Эти меры направлены на предупреждение инфекционных осложнений. В случае развития некротической энтеропатии осуществляется перевод больного на парентеральное питание. Пациентам с агранулоцитозом необходим тщательный уход за полостью рта (частые полоскания рта антисептическими растворами, смазывание слизистых оболочек).
Терапия агранулоцитоза начинается с устранения этиологического фактора (отмены миелотоксических препаратов и химических веществ и т. д.). Для профилактики гнойной инфекции назначаются неабсорбируемые антибиотики, противогрибковые препараты. Показано внутривенное введение иммуноглобулина и антистафилококковой плазмы, трансфузии лейкоцитарной массы, при геморрагическом синдроме - тромбоцитарной массы. При иммунном и аутоиммунном характере агранулоцитоза назначаются глюкортикоиды в высоких дозах. При наличии в крови ЦИК и антител проводится плазмаферез. В комплексном лечении агранулоцитоза используются стимуляторы лейкопоэза.
Профилактика агранулоцитоза, главным образом, заключается в проведении тщательного гематологического контроля во время курса лечения миелотоксическими препаратами, исключении повторного приема лекарств, ранее вызвавших у больного явления иммунного агранулоцитоза. Неблагоприятный прогноз наблюдается при развитии тяжелых септических осложнений, повторном развитии гаптеновых агранулоцитозов.
www.krasotaimedicina.ru
Вопрос 39. Агранулоцитоз: классификация, виды, причины, механизмы развития, клинические проявления. Картина периферической крови при агранулоцитозе. Панмиелофтиз.
Агранулоцитозы — состояние, характеризующееся значительным снижением количества гранулоцитов, в основном нейтрофилов, или их полным отсутствием в периферической крови.
Агранулоцитоз, в подавляющем большинстве случаев является синдромом какого-то общего заболевания. Более распространены миелотоксический агранулоцитоз ( цитостатический эффект) и иммунный. Последний возникает в результате аутоиммунной агрессии (например, при системной красной волчанке) и антител к гранулоцитам после приема медикаментов, оказавшихся гаптенами (при попадании в организм эти медикаменты, соединяясь с белком, обретают свойства антигена).
Классификация
приобретенные
врожденные формы
Первые могут встречаться в виде самостоятельного заболевания или быть одним из синдромов, сопровождающих течение различных патологических процессов.
По клиническому течению дифференцируют
По патогенезу
а) миелотоксические
б) иммунные.
Различают также агранулоцитозы, в возникновении которых имеют значение определенный этиологический фактор и идиопатические формы с неустановленной этиологией.
Миелотоксические агранулоцитозы
Миелотоксические агранулоцитозы возникают в результате подавления роста предстадий гранулоцитов в костном мозге, включая и стволовые клетки. В связи с этим в крови отмечается уменьшение не только гранулоцитов, но и тромбоцитов, ретикулоцитов и лимфоцитов. Миелотоксический агранулоцитоз может развиться в результате воздействия на организм ионизирующей радиации, химических соединений, обладающих цитостатическими свойствами (противоопухолевые препараты, бензол и других), продуктов жизнедеятельности грибка типа Fusarium, размножающегося в перезимовавшем зерне.
Иммунный агранулоцитоз
Иммунный агранулоцитоз развивается в результате ускоренной гибели гранулоцитов под влиянием антилейкоцитарных антител; стволовые клетки не страдают. Антилейкоцитарные антитела образуются под влиянием медикаментов, могущих играть роль гаптенов. При повторном введении такого медикамента появляется агглютинация лейкоцитов.
Развитие иммунного агранулоцитоза мало зависит от дозы препарата, важнейшую роль в его возникновении играет необычная чувствительность организма. Напротив, при миелотокснческом агранулоцитозе решающая роль принадлежит величине повреждающего воздействия. Среди лекарств, вызывающих иммунный агранулоцитоз, основное место принадлежит амидопирину. Иммунный агранулоцитоз, кроме того, могут вызвать бутадион, фенацетин, атофан, анальгин, диакарб, барбамил, сульфаниламиды, ПАСК, тубазид, этоксид, стрептомицин, пипольфен и некоторые другие препараты. Продолжительный прием препарата гаптена может вызвать разрушение не только зрелых гранулоцитов, но и миелоцитов и промиелоцитов. Развитие аутоиммунного агранулоцитоза, чаще лейкопении, наблюдается при коллагенозах (особенно рассеянной красной волчанке, ревматоидном полиартрите), а также при некоторых инфекциях.
Особое место занимают агранулоцитозы при системных поражениях кроветворного аппарата — лейкозах, гипопластической анемии, а также при метастазах в костный мозг раковой опухоли и саркомы.
Клиника
Основные клинико-гематологические признаки острых агранулоцитозов: выраженная интоксикация на фоне ангины, афтозного стоматита, язвенно-некротического поражения небных дужек, язычка, твердого неба, десен, иногда желудочно-кишечного тракта, легких, печени, половых органов; нередко отмечают увеличение регионарных лимфатических узлов (шейные, подчелюстные и др.); глубокие изъязвления тканей могут сопровождаться обильными кровотечениями из разрушенных сосудов; при некротической энтеропатии возможно развитие перфорации кишки и перитонита; пневмонии отличаются скудными физическими и рентгенологическими данными; нередко встречаются нарушения функции печени и почек. Поражение гранулоцитопоэза, как правило, характеризуется абсолютной нейтропенией и снижением абсолютного количества лейкоцитов; в гемограмме могут встречаться единичные бластные и плазматические клетки, увеличено количество эозинофилов; в миелограмме обычно преобладают промиелоциты и миелоциты, число зрелых нейтрофилов снижено вплоть до полного отсутствия, обнаруживаются относительный лимфоцитоз и увеличение числа плазматических клеток; нередко наблюдаются также изменения эритро- и тромбоцитопоэза.
Хронические нейтропении представляют собой отдельную нозологическую форму или синдром при различных заболеваниях. Среди них выделяют идиопатическую форму с отсутствием указаний на воздействие какого-либо этиологического фактора и требующую лечения лишь при диагностированных инфекциях. Иммунная форма по своему патогенезу не отличается от механизма развития острых иммунных нейтропении.
Врожденные нейтропении по своему патогенезу и клинико-гематологической картине представляют собой гетерогенную группу заболеваний. Приводим некоторые из них.
Инфантильный генетический агранулоцитоз (болезнь Костмана) наследуется по аутосомно-рецессивному типу. Характерными признаками являются тяжелые инфекции, приводящие к гибели больных через 5—10 мес. после рождения, абсолютная глубокая нейтропения, в миелограмме преобладают промиелоциты, более зрелые гранулоциты практически отсутствуют. Механизм развития гранулоцитопении обусловлен дефектом гемопоэтических стволовых клеток.
Наследственная нейтропения — заболевание аутосомно-доминантного типа, отличается доброкачественным течением. Склонность к инфекциям проявляется с первых месяцев жизни и с возрастом стихает. Патогенез развития нейтропении при различных вариантах заболевания не однозначен (нарушение созревания нейтрофилов в костном мозге, торможение поступления их в периферическую кровь, иммунные и регуляторные расстройства и др.).
Циклическая нейтропения также наследуется по аутосомно-доминантному типу, обычно проявляется в раннем детстве или юности. Как правило, в течение 3—5 дней наблюдаются выраженная нейтропения, лихорадка, инфекции, затем в среднем к 21-му дню больные практически выздоравливают. Прогноз относительно благоприятный, с возрастом клиническая симптоматика стихает. В основе патогенеза лежит ингибиция пролиферации стволовых клеток зрелыми нейтрофилами костного мозга, не исключается и дефект на уровне гемопоэтических стволовых клеток.
Вопрос 40-42. Лейкозы: определение понятия, общая характеристика, принципы классификации. Лейкозы: характеристика основных клинических синдромов лейкозов. Характеристика основных теорий этиологии лейкозов. Основные стадии патогенеза лейкозов.
Лейкоз – опухоль кроветворной системы, первично поражающая кроветворные клетки костного мозга. При этом в процесс вторично вовлекаются периферическая кровь и другие ткани, особенно ткани РЭС (ретикуло-эндотелиальной системы).
По течению заболевания лейкозы подразделяют на две основные группы – острые и хронические.
Этиология.
Вероятнее всего, что лейкоз является мультифакторным заболеванием, в его возникновении играют роль и внешние и внутренние факторы, причём все они вызывают не сам лейкоз, а повышенную мутабельность в ткани, из которой в дальнейшем может (но не обязательно!) развиться опухоль.
Существует несколько теорий происхождения лейкозов.
Радиационная теория. Роль ионизирующих излучений в возникновении лейкозов доказана в эксперименте. Как однократное (в дозе 2 Гр и выше), так и хроническое (в течение 2–3 месяцев) облучение лучами Рентгена в малых дозах может индуцировать лейкоз у лабораторных животных (крысы, мыши). Прослежено повышение заболеваемости острым и хроническим миелолейкозом у жителей Хиросимы и Нагасаки, у рентгенологов и радиологов. Приводятся данные об увеличении частоты лейкозов у больных, леченных большими дозами лучей Рентгена, иттрия, радия по поводу злокачественных новообразований и анкилозирующего спондилоартрита, а также у детей, получавших облучение вилочковой железы в раннем возрасте, и др. Описано учащение случаев острых лейкозов среди больных эритремией после лечения их радиоактивным фосфором.
Теория химического лейкозогенеза. Экспериментально доказана возможность индуцирования лейкозов у животных введением канцерогенных веществ (диметилбензантрацен, метилхолантрен и др.). Также в эксперименте показана возможность стимуляции лейкозогенеза метаболитами триптофана и тирозина (М.Л. Раушенбах). Однако роль этих веществ в лейкозогенезе человека не доказана. В то же время накоплены данные, указывающие на увеличение риска заболевания лейкозами (как правило, острыми) у людей, имеющих длительный профессиональный контакт с бензолом и летучими органическими растворителями (шоферы, работники кожевенной и обувной промышленности и т.д.). В последние годы отмечено заметное учащение случаев острого лейкоза у больных злокачественными новообразованиями, леченных такими цитостатическими препаратами, как циклосфосфан, хлорбутин, метотрексат, миелосан, адриамицин и др. К лекарственным препаратам, способным индуцировать лейкозы, относятся также бутадиен, левомицетин и некоторые другие.
Вирусная теория связывает возникновение лейкозов с активацией (под действием радиации и химических факторов) латентных лейкозогенных вирусов. Несомненно, доказанным является вирусное происхождение лейкозов у многих видов животных птиц, мышей, крыс, хомячков, кошек, крупного рогатого скота. К настоящему времени выделено и детально охарактеризовано несколько типов вирусов, вызывающих различные виды лейкозов у животных. Как правило, это РНК-содержащие вирусы, а также ДНК-содержащие вирусы, которые относятся к герпесвирусам.
Вопрос о роли вирусов в происхождении лейкозов у человека остается во многом спорным. Против вирусной этиологии лейкозов у человека свидетельствует, прежде всего, факт невозможности прямой перевивки лейкозов при случайном переливании крови лиц, больных лейкозом, и отсутствие убедительных доказательств контагиозное лейкозов. Не описаны также случаи передачи лейкоза от больной матери плоду и новорожденному в период вскармливания грудью. Генетическая теория располагает достаточно убедительными аргументами, указывающими на возможность наследственной предрасположенности к лейкозам. Известны случаи семейных лейкозов, доказана роль этнических особенностей в развитии лимфолейкоза. К возникновению лейкозов предрасполагают болезни, характеризующиеся спонтанными разрывами хромосом и нерасхождением соматических или половых хромосом (болезнь Дауна, анемия Фанкони, синдромы Кляйнфелтера, Тернера и др.). Получены линии мышей, у которых частота спонтанных лейкозов близка к 100 %.
studfiles.net
Агранулоцитоз
Агранулоцитоз – клинико-лабораторный синдром, основное проявление которого состоит в резком снижении или полном отсутствии нейтрофильных гранулоцитов в периферической крови, что сопровождается повышением восприимчивости организма к грибковым и бактериальным инфекциям.
 Агранулоцитоз характеризуется резким снижением гранулоцитов в периферической крови
Агранулоцитоз характеризуется резким снижением гранулоцитов в периферической крови Гранулоциты – это наиболее многочисленная группа лейкоцитов, у которых при окрашивании в цитоплазме становятся заметными специфические гранулы (зернистость). Данные клетки относятся к миелоидным и вырабатываются в костном мозге. Гранулоциты принимают активное участие в защите организма от инфекций: при проникновении инфекционного агента в ткани они мигрируют из кровеносного русла через капиллярные стенки и устремляются в очаг воспаления, здесь поглощают бактерии или грибки, а затем разрушают их своими ферментами. Обозначенный процесс приводит к формированию местного воспалительного ответа.
При агранулоцитозе организм не в состоянии противостоять инфекции, что нередко становится фактором возникновения гнойно-септических осложнений.
У мужчин агранулоцитоз диагностируется в 2-3 раза реже, чем у женщин; наиболее подвержены ему люди старше 40 лет.
Причины
При аутоиммунной форме синдрома в функционировании иммунной системы происходит определенный сбой, в результате чего она вырабатывает антитела (так называемые аутоантитела), атакующие гранулоциты, вызывая тем самым их гибель. Аутоиммунный агранулоцитоз может возникать на фоне следующих заболеваний:
- аутоиммунный тиреоидит;
- системная красная волчанка;
- ревматоидный артрит и другие виды коллагенозов.
 Системная красная волчанка – одна из причин аутоиммунного агранулоцитоза
Системная красная волчанка – одна из причин аутоиммунного агранулоцитоза Иммунный характер имеет и агранулоцитоз, развивающийся как осложнение инфекционных заболеваний, в частности:
- полиомиелита;
- вирусных гепатитов;
- брюшного тифа;
- желтой лихорадки;
- малярии;
- инфекционного мононуклеоза;
- гриппа.
В настоящее время нередко диагностируется гаптеновая форма агранулоцитоза. Гаптенами называются химические вещества, молекулярная масса которых не превышает 10 000 Да. К ним относятся многие лекарственные препараты. Гаптены сами по себе не обладают иммуногенностью и приобретают это свойство только после соединения с антителами. Образовавшиеся соединения могут оказывать токсическое воздействие на гранулоциты, вызывая их гибель. Однажды развившийся гаптеновый агранулоцитоз будет повторяться каждый раз при приеме того же гаптена (лекарственного средства). Наиболее часто причиной гаптенового агранулоцитоза становятся препараты Диакарб, Амидопирин, Антипирин, Анальгин, Аспирин, Изониазид, Мепробамат, Бутадион, Фенацетин, Индометацин, Новокаинамид, Левамизол, Метициллин, Бактрим и другие сульфаниламиды, Лепонекс, Хлорохин, барбитураты.
Миелотоксический агранулоцитоз возникает в результате нарушения процесса миелопоэза, протекающего в костном мозге и связанного с подавлением продукции клеток-предшественников. Развитие названной формы сопряжено с воздействием на организм цитостатических средств, ионизирующего излучения и некоторых медикаментов (Пенициллина, Гентамицина, Стрептомицина, Левомицетина, Аминазина, Колхицина). При миелотоксическом агранулоцитозе в крови снижается количество не только гранулоцитов, но и тромбоцитов, ретикулоцитов, лимфоцитов, поэтому данное состояние называют цитотоксической болезнью.
С целью снижения риска инфекционно-воспалительных заболеваний лечение пациентов с подтвержденным агранулоцитозом проводят в асептическом блоке гематологического отделения.Формы
Агранулоцитоз бывает врожденным и приобретенным. Врожденный связан с генетическими факторами и встречается крайне редко.
Приобретенные формы агранулоцитоза выявляются с частотой 1 случай на 1300 человек. Выше описывалось, что, в зависимости от особенностей патологического механизма, лежащего в основе гибели гранулоцитов, выделяют следующие его виды:
- миелотоксический (цитотоксическая болезнь);
- аутоиммунный;
- гаптеновый (лекарственный).
Известна также генуинная (идиопатическая) форма, при которой причину развития агранулоцитоза установить не удается.
По характеру течения агранулоцитоз бывает острым и хроническим.
Признаки
Первыми симптомами агранулоцитоза являются:
- резкая слабость;
- бледность кожных покровов;
- боли в суставах;
- повышенная потливость;
- повышенная температура тела (до 39–40 °C).
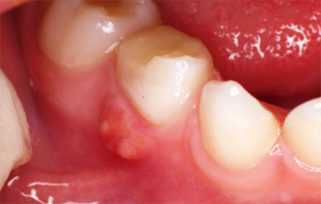
Характерны язвенно-некротические поражения слизистой оболочки ротовой полости и глотки, которые могут иметь вид следующих заболеваний:
- ангина;
- фарингит;
- стоматит;
- гингивит;
- некротизация твердого и мягкого неба, язычка.
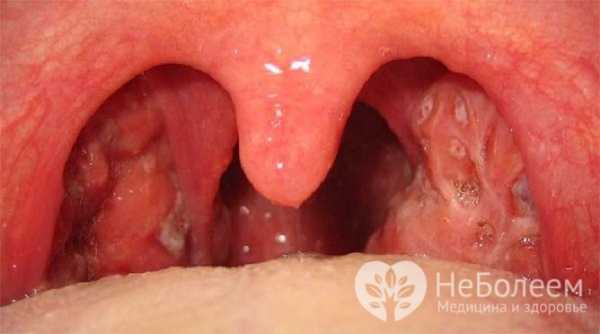 Язвенно-некротические поражения слизистой оболочки полости характерны для агранулоцитоза
Язвенно-некротические поражения слизистой оболочки полости характерны для агранулоцитоза Эти процессы сопровождаются спазмом жевательной мускулатуры, затруднениями глотания, болью в горле, повышенным слюнотечением.
При агранулоцитозе происходит увеличение селезенки и печени, развивается регионарный лимфаденит.
Особенности протекания миелотоксического агранулоцитоза
Для миелотоксического агранулоцитоза, помимо перечисленных выше симптомов, характерен умеренно выраженный геморрагический синдром:
- образование гематом;
- носовые кровотечения;
- повышенная кровоточивость десен;
- гематурия;
- рвота с примесью крови либо в виде «кофейной гущи»;
- видимая алая кровь в каловых массах или черный дегтеобразный стул (мелена).
Синдром хронической усталости – болезнь XXI века
6 правил приема антибиотиков
Морские водоросли: 6 причин для включения в рацион
Диагностика
Для подтверждения агранулоцитоза проводят общий анализ крови и пункцию костного мозга.
 Для диагностики агранулоцитоза проводят общий анализ крови
Для диагностики агранулоцитоза проводят общий анализ крови В общем анализе крови определяется выраженная лейкопения, при которой общее количество лейкоцитов не превышает 1–2 х 109/л (норма – 4–9 х 109/л). При этом либо вообще не определяются гранулоциты, либо их количество оказывается менее 0,75 х 109/л (норма – 47–75% от общего количества лейкоцитов).
При исследовании клеточного состава костного мозга выявляются:
- снижение количества миелокариоцитов;
- увеличение количества мегакариоцитов и плазматических клеток;
- нарушение созревания и снижение числа клеток нейтрофильного ростка.
Для подтверждения аутоиммунного агранулоцитоза проводят определение наличия антинейтрофильных антител.
При выявлении агранулоцитоза пациент должен быть проконсультирован отоларингологом и стоматологом. Помимо этого, ему нужно пройти трехкратное исследование крови на стерильность, биохимический анализ крови и рентгенографию легких.
Агранулоцитоз требует дифференциальной диагностики с гипопластической анемией, острым лейкозом, ВИЧ-инфекцией.
Агранулоцитоз бывает врожденным и приобретенным, причем, первая форма – крайне редкое явления и обуславливается наследственными факторами.Лечение
Лечение пациентов с подтвержденным агранулоцитозом проводят в асептическом блоке гематологического отделения, что существенно снижает риск инфекционно-воспалительных осложнений. В первую очередь необходимо выявить и устранить причину агранулоцитоза, например, отменить цитостатический препарат.
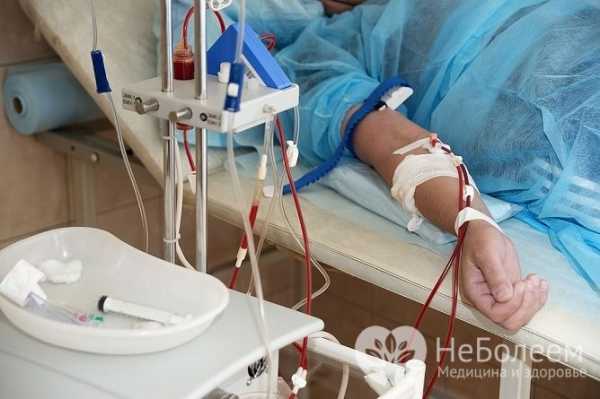 Для лечения агранулоцитоза показан плазмаферез
Для лечения агранулоцитоза показан плазмаферез При агранулоцитозе иммунного характера обязательно назначают высокие дозы глюкокортикоидных гормонов, проводят плазмаферез. Показаны трансфузии лейкоцитарной массы, внутривенное введение антистафилококковой плазмы и иммуноглобулина. Для увеличения выработки гранулоцитов в костном мозге нужно принимать стимуляторы лейкопоэза.
Также назначаются регулярные полоскания рта антисептическими растворами.
При возникновении некротической энтеропатии больных переводят на парентеральное питание (питательные вещества вводят путем внутривенной инфузии растворов, содержащих аминокислоты, глюкозу, электролиты и т. п.).
В целях профилактики вторичной инфекции применяют антибиотики и противогрибковые препараты.
Прогноз значительно ухудшается при развитии тяжелых септических состояний, а также в случае повторных эпизодов гаптенового агранулоцитоза.Профилактика
Без назначения врача и тщательного гематологического контроля недопустимо принимать лекарственные препараты, обладающие миелотоксическим действием.
Если зафиксирован эпизод гаптенового агранулоцитоза, в дальнейшем не следует принимать препарат, послуживший причиной его развития.
Последствия и осложнения
Наиболее частыми осложнениями агранулоцитоза являются:
- пневмония;
- геморрагия;
- гепатит;
- сепсис;
- медиастинит;
- перитонит.
Прогноз значительно ухудшается при развитии тяжелых септических состояний, а также в случае повторных эпизодов гаптенового агранулоцитоза.
Видео с YouTube по теме статьи:
www.neboleem.net
Симптомы агранулоцитоза
При агранулоцитозе характерным симптомом считается формирование язв, причём с высокой скоростью. Некротизация тканей распространяется не только на поражённых участках, но и на соседних поверхностях. При этом данный процесс может приобрести проявления номы, то есть водяного рака, при котором данный патологический процесс переходит на слизистую оболочку щёк, что вызывает гангренозные осложнения в тканях лица.
Такие же воспаления затрагивают и желудочно-кишечный тракт, в котором возникают проявления язвенно-некротической энтеропатии. При этом процессе образуются некрозы слизистой оболочки таких органов, как пищевод, желудок и кишечник. Симптомы данного заболевания выражаются в появлении поносов, в некоторых случаях, с кровью и рвоты. При сильной стадии некротических поражений эпителия желудочно-кишечного тракта появляются сильные кровотечения, которые представляют угрозу жизни человека.
У некоторых больных возможно развитие желтухи, поскольку печень также претерпевает поражения тканей.
Иногда, но достаточно редко, возможно перфорирование язв, при которых появляются все клинические симптомы «острого живота».
Возможно, также, и возникновение пневмонии, которое протекает довольно нетипично – с появлением нарывов (абсцессов), развитием гангрены и проникновением патологического процесса в ткани соседних органов. При этом больного начинают беспокоить такие симптомы, как кашель, одышка и боли в груди (если началось поражение плевры). Тяжёлые случаи заболевания сопровождает такое явление, как острая дыхательная недостаточность.
Иногда при агранулоцитозе возникают заболевания мочеполовой системы инфекционной природы, которые затрагивают уретру и мочевой пузырь, а у женщин – матку и влагалище. При этом характерно ощущение рези и болезненных ощущений во время мочеиспускания, а также болей внизу живота. Женщины также могут жаловаться на появление зуда и патологических выделений из влагалища.
Процессы интоксикации при агранулоцитозе начинают запускать артериальную и венозную гипотонию. Если же проводится аускультация сердца, то при этом можно обнаружить появление функциональных шумов.
Процессы в почках характеризуются симптомом альбуминурия, то есть выделения вместе с мочой повышенного количества белка. Такие изменения вызваны реакцией организма на процессы распространения инфекций. Если же почки затронуты инфицированием посредством проникновения патологических микроорганизмов из мочевыводящих путей, то в моче можно наблюдать появление крови, а также белка и клеток, которым выстлан эпителий почечных канальцев.
[1], [2], [3], [4]
ilive.com.ua
Миелотоксический агранулоцитоз: признаки
Миелотоксический агранулоцитоз подразумевает собой снижение лейкоцитов, за счет агранулоцитов и лимфоцитов. Происходит это в результате недостаточной работы костного мозга. Страдает костный росток – зона, где продуцируются гранулоциты. Подавленная работа органа кроветворения может быть вызвана действием различных причин, которые мы разберем подробнее.
Миелотоксический агранулоцитоз
Классификация: кратко
Патологию делят на формы: эндогенный и экзогенный миелотоксический агранулоцитоз. В первом случае синдром развивается в результате воздействия на организм причин извне (из окружающей среды), во втором – под воздействием заболеваний-первопричин (цитостатической болезни). Экзогенный миелотоксический агранулоцитоз является лишь как манифестирующий симптом другой патологии.
Патология может быть врожденным или приобретенным синдромом. Иногда его диагностируют у младенцев еще в родильном доме, но чаще миелотоксический агранулоцитоз – удел более старшего населения нашей страны. Синдром может принимать острое или рецидивирующее течение. По степени тяжести различают: легкую, среднюю, тяжелую степень.
Причины возникновения недуга
Миелотоксический агранулоцитоз может развиться в результате действия отравляющих веществ, особенно при соприкосновении с ртутью или ее парами. Вредным для костного мозга действием обладает повышенная доза радиации, что часто встречается при лучевом лечении онкологических больных. Врожденный миелотоксический агранулоцитоз зачастую носит генетический характер.
Цитостатический эффект оказывают множество заболеваний. К ним относится: вирус Эпстайна – Барра, цитомегаловирус, желтая лихорадка, гепатиты вирусного генеза. Миелотоксический агранулоцитоз вызывают и генерализованные инфекции, имеющие не только бактериальную, но и вирусную природу. Быстрое похудение, с применением несвойтсвенных для организма методик, в редких случаях сопровождается падением лейкоцитов в крови. Это нужно учитывать при нормализации веса.
Симптомы и диагностика
Характерные признаки болезни – снижение защитных сил организма, присоединение грибковых и инфекционных патологий. В данном случае восприимчивость организма к инфекциям возрастает вдвое, а то и втрое. Этот сдвиг в формуле крови и объясняет резкое падение иммунитета, а также проявлений внешних признаков инфекции. Особенно если иммунитет был ослаблен еще до инфицирования, то в таком случае ухудшение состояния здоровья пациента происходит просто молниеносно. Это не благотворно влияет на течение болезни и успех ее дальнейшего лечения.
При миелотоксической форме агранулоцитоза появляется патологическая кровоточивость, образование гематом, гематурия. Кожа покрывается кровоподтеками различной степени давности. Синяки имеют различный окрас, зависящий от степени их давности. Присоединяется кровоточивость десен, которая по мере развития формы синдрома, становится все интенсивнее. Под поражение попадает кишечник, диагностируют некротическую энтеропатию. Данная патология может иметь тяжелые последствия для организма – прободения (разрыв) кишки, перетониты (воспаление брюшины), сепсис (общее заражение крови). Наряду с кишечником могут пострадать легкие и проявиться геморрагическая пневмония.
Диагностика
Диагностируют патологический синдром путем проведения общего анализа крови. В результатах исследования периферической крови находят лейкопению, гранулоцитопению, анемию умеренной степени, тромбоцитопению (в запущенных случаях). В пунктате костного мозга снижается количество миелокариоцитов, клеток нейтрофильного роста. Вырастает численность мегакариоцитов и плазматических клеток. Из других исследований может дополнительно потребоваться:
- пункция спинного мозга;
- рентгенография ОГП (органов грудной клетки). Она позволит узнать состояние легких, дабы заранее диагностировать пневмонии;
- биохимия крови;
- общий анализ мочи;
- исследование на ВИЧ;
- по необходимости и в зависимости от жалоб требуется консультация смежных специалистов, чаще это отоларинголог, стоматолог, гастроэнтеролог.
Лечение
Для болезни характерны два типа лечения: комплексное и этиотропное (нацеленное на конкретную причину). Только специалист может правильно подобрать терапевтическую схему. Делают это после тщательной, всесторонней диагностики и сбора результатов всех исследований. Комплексная терапия подразумевает под собой ряд таких мероприятий:
- убираем причину, которая привела к снижению агранулоцитов.
- Создаем условия тотальной стерильности (во избежание параллельного заражения инфекциями).
- Активная профилактика осложнений (для этого нужен постоянный мониторинг всех показателей).
- Переливание крови (для стимуляции выработки агранулоцитов организмом).
- Назначение антибиотиков. Показано для терапии или профилактики гнойных патологий.
- Мероприятия для снижения проявлений интоксикации (дезинтоксикационная терапия).
- Стимуляторы лейкопоэза.
- Плазмаферез (в некоторых случаях).
- Переливание тромбоцитарной массы.
- Внутривенные инфузии иммуноглобулина, антистафилококковой массы.
- Стероидное (гормональное) лечение в высоких дозировках.
Этиотропное лечение направляют на устранение причины заболевания и последующее прекращение ее влияния на кроветворную систему. Успех лечения всех типов агранулоцтозов заключаются в устранении основных симптомов. Также требуется максимальное стимулирование иммунитета для достижения ремиссий. Известно, что выявление болезни на раннем этапе – это уже гарантия максимально действенного и успешного лечения. Успех терапии удваивается, если оно происходит в соответствии с формами болезни.
Течение и прогноз
Миелотоксический агранулоцитоз развивается либо остро, либо же постепенно. Нужно учитывать, что именно характерно в причине заболевания. Острое проявление значительно усложняет лечебный процесс, так как жизненные показатели меняются динамически, и они могут быть абсолютно разными на протяжении даже нескольких часов.
В молниеносном течении благоприятный прогноз — это следствие снижения количества агранулоцитов и качественной медицинской помощи. Еще важен факт наличия полного обследования, дабы не пропустить ничего существенного, что может спровоцировать рецидив болезни (повторное ухудшение для пациента). При хроническом течении болезни учитывается факт успешной ликвидации причины подобного состояния (например: отравление ртутью).
Агранулоцитоз причины - формы и признаки - диагностика, лечение, профилактикаТема: Болезни - Агранулоцитоз. Видео №1А вот этот тип болезни зачастую встречается у людей, которые работают с опасными веществами без строжайшего соблюдения техники безопасности. Стоит учесть, что отравление такими веществами не должно быть одноразовым. Известны случаи, когда яд накапливался со временем, потому симптомы были вялотекущими.
Выводы
Некоторые формы миелотоксического агранулоцитоза могут проявлять себя наследственно. Поэтому, доктору особое внимание стоит обращать на анамнез (совокупность сведений о состоянии здоровья и жизни пациента) абсолютно всех членов семьи. Болезнь легче предотвратить и остановить на ранней стадии. Врачи рекомендуют обследоваться и регулярно сдавать анализы, для избежание плачевных последствий.
Если вы заметили у себя или у своего ребенка первые, даже незначительные симптомы болезни, то откладывать с визитом к специалисту нельзя. Срочно обратитесь к врачу, ведь лучше посетить его заранее и потратить пару часов на обследование и анализы, чем рисковать своим здоровьем из-за халатности.
kakiebolezni.ru
АГРАНУЛОЦИТОЗ
Этот файл взят из коллекции Medinfo
http://www.doktor.ru/medinfo
http://medinfo.home.ml.org
E-mail: [email protected]
FidoNet 2:5030/434 Andrey Novicov
Пишем рефераты на заказ - e-mail: [email protected]
В Medinfo для вас самая большая русская коллекция медицинских
рефератов, историй болезни, литературы, обучающих программ, тестов.
Заходите на http://www.doktor.ru - Русский медицинский сервер для всех!
ЛЕКЦИЯ ПО ВНУТРЕННИМ БОЛЕЗНЯМ. 2 СЕМЕСТР. 5 КУРС.
ЛЕКЦИЯ №2.
ТЕМА: АГРАНУЛОЦИТОЗ. ПАРЦИАЛЬНАЯ АПЛАЗИЯ. МИЕЛОМНАЯ БОЛЕЗНЬ.
Агранулоцитоз - клинико-гематологический синдром, описанный впервые в 1922 году Шульцом. Агранулоцитоз был описан реакция на амидопирин. Данное состояние характеризуется полным или практически полным исчезновением нейтрофильных гранулоцитов в периферической крови (1.2 - 1.7 тысячи) и инфекционными осложнениями. Смертность составляет от 3 до 36%. Частота встречаемости 1 на 1200 человек. Интересно отметить, что агранулоцитоз чаще болеют женщины, старше 40 лет.
Этиология.
-
медикаменты (60%). Агранулоцитоз могут вызвать примерно 300 препаратов. Чаще всего вызвает развитие агранулоцитоза:
-
пиразолоновый ряд ненаркотических анальгетиков (анальгин, бисептол и др.). данные препараты вызывают агранулоцитоз гаптенового генеза. Необходимо учитывать, что агранулоцитоз развивается независимо от дозы препарата.
-
сульфаниламиды и антибиотики
-
противотуберкулезные препараты
-
снотворные
-
транквилизаторы
-
вакцины
-
цитостатики. Однако при приеме цитостатиков мы ожидаем развитие агранулоцитоза, который является закономерной реакцией на данную терапию. Эффект от цитостатической терапии напрямую связан с дозой.
-
химические вещества (бензин, бензол, алкоголь)
-
вирусные инфекции (гепатиты, грипп, инфекционный мононуклеоз). Кроме того инфекция протекает с аллергическим компонентом и является предрасполагающим фактором к развитию агранулоцитоза.
-
идиопатический (нет явной причины).
Острый агранулоцитоз. Бывает двух вариантов - 1)миелотоксический (вследствие воздействия цитостатических препаратов, ионизирующего излучения, когда оказывается прямое действие на клетки гранулопоэза, и на стволовую клетку предшественницу гранулопоэза) и 2)аутоиммунный.
Среди аутоимунных агранулоцитозов выделяют:
-
симптоматические, то есть агранулоцитоз (является симптомом какого-либо заболевания - синдром Фелти - это вариант ревматоидного полиартрита, при котором кроме суставного синдрома имеется спленомегалия и агранулоцитоз, вследствие гиперспленизма).
-
Приобретенные аутоиммунные агранулоцитозы, как правило, гаптенового генеза. В этом случае лекарственный препарат сам по себе не обладающий миелотоксическим эффектом начинает играть роль гаптена, при этом провоцируя выработку клона лимфоцитов, обладающих киллерным действием на клетки миелоидного ростка, в частности на клетки миелопоэза. К этим препаратам относятся препараты, которые широко используются в клинической практике - анальгетики (анальгин, баралгин, пенталгин), сульфаниламиды (бисептол), противодиабетические препараты, антитиреоидные препараты (мерказолил), хлорамфеникол (левомицетин).
Дадим сравнительную характеристику аутоиммунному и миелотоксическому агранулоцитозу.
| Признак | аутоиммунный (иммунный) | миелотоксический |
| Уровень поражения клеток | различный (могут поражаться ранние клетки, могут поражаться зрелые или созревающие клетки). Однако, чаще антитела образуются к зрелым клеткам. | Погибают пролиферирующие, ранние клетки. Зрелые клетки некоторое время циркулируют в крови. |
| Поражение ростков | антитела направлены только на нейтрофилы | Трехростковый |
| Скорость развития агранулоцитоза | очень быстро (часы), так как сразу погибают зрелые клетки | развивается через несколько дней |
| Выход из агранулоцитоза | быстрый | минимум 2 недели |
| Связь с дозой воздействия | не связан | напрямую связан с дозой |
| Сохранность ранних клеток | сохранены | снижаются в первую очередь |
| Механизм развития | гибель клеток происходит под действием антител. В этом случае лекарство является гаптеном. Происходит лизис нейтрофилов. Если участвует комплемент, то идет комплексное иммунное повреждение, то есть образование циркулирующих иммунных комплексов. Пример: если здоровому человеку ввести плазму больного , то у него разовьется агранулоцитоз. | Происходит нарушение внутриклеточного метаболизма и нарушение пролиферации. |
| Факторы, вызывающие агранулоцитоз | развивается на фоне системных заболеваний соединительной ткани (СКВ, ревматоидный артрит), хронический гломерулонефрит, миелома, лимфома. | Чаще всего вызывает аминазин (прямое токсическое воздействие), цитостатики, мерказолил (однако при его приеме имеет место неблагоприятный статус больного), левомицетин ( в данном случае важен генетический фон). Может быть индивидуальная идиосинкразия (ферментные дефекты врожденного характера: это касается самих гранулоцитов). Может быть нарушение метаболизма лекарств из-за дефекта печеночных клеток, нарушения выведения продуктов метаболизма лекарственных веществ из-за патологии почек. |
Редко встречается циклическое течение (циклическая форма агранулоцитоза): 3-4 дня агранулоцитоз, затем перерыв 21 день, а потом опять все повторяется. Патогенез не ясен. Вероятен иммунный компонент.
Рецидив агранулоцитоза свойственен для всех форм, однако, механизмы рецидивов не всегда ясны.
Необходимо делать стернальную пункцию, чтобы знать состояние ростка.
Клинико-гематологическая картина агранулоцитоза.
Главное клиническое проявление - инфекционное заболевание, интоксикация.
Формы агранулоцитоза:
-
острейший, молниеносный агранулоцитоз
-
острый агранулоцитоз
-
подострый агранулоцитоз при затяжном течении
-
рецидивирующий
-
циклический
Тяжесть инфекционных осложнений определяется длительностью агранулоцитоза. Глубина агранулоцитоза: о-нейтрофилов - инфекция развивается впервые дни; 0.3 - 0.5 на 109/л - тяжелая инфекция без некрозов; 0.5 - 0.75 на 109 (1000 лейкоцитов) - инфекции может не быть впервые 2 недели.
Начало агранулоцитоза: острое и быстрое развитие симптоматики. Иногда может быть продрома. Развивается лихорадка, головная боль, озноб, слабость, боль при глотании. Инфекции слизистых входных ворот - ангина, стоматит. Также характерно развитие пневмонии и поражение кишечника, что ведет к развитию сепсиса. Иногда развиваются деструктивные некротические инфекции, абсцессы легкого. С хирургическим вмешательством не торопиться, так как гноя нет!. Может быть:
-
некротическая энтеропатия, которая характеризуется схваткообразными болями в животе, диареей, метеоризмом, интоксикацией. В илеоцекальной области - плеск, урчание. Данная патология часто развивается при цитостатическом агранулоцитозе.
-
ишемический энтероколит
-
язвенно-некротический энтероколит
-
геморрагический энтероколит
-
перфорация с перитонитом и шоком. Клинические проявления не очень яркие (боли летучие, симптомы раздражения брюшины слабые).
Поражение органов дыхания. Скудная физикальная и рентгенологическая картина пневмонии. Хрипов нет, несколько ослаблено дыхание. Нет инфильтрации на рентгене, так как нет субстанции (нейтрофилов).
Сердечно-сосудистая система: развитие гипотонии или шока.
Также нарушается функция почек. Увеличиваеются лимфатические узлы около очага инфекции. Часто развивается токсический гепатит (к развитию гепатита, как правило, ведет прием циклофосфана, мерказолила, аминазина). Имеет место увеличение селезенки.
Гемограмма.
Резко снижено количество нейтрофилов. При дальнейшем развитии агранулоцитоза снижается количество эозинофило и базофилов. Остаются лимфоциты. При выходе из агранулоцитоза появляются моноциты, единичные миелоциты, зрелые гранулоциты. За неделю гемограмма приходит к норме.
Аутоиммунный агранулоцитоз: количество лейкоцитов 1-2 на 109/л за счет лимфоцитов и единичных гранулоцитов. Часто развивается анемия, тромбоцитопения. Характерны морфологические и функциональные изменения лейкоцитов: токсическая зернистость, пикноз ядер, нарушение фагоцитоза, уменьшение содержания гликогена, липидов и ферментов.
Костный мозг: изолированное нарушение гранулоцитопоэза: может быть несколько вариантов нарушения:
-
депрессия гранулоцитов зрелых + омоложение. Такая ситуация наблюдается при входе , или выходе из агранулоцитоза.
-
депрессия гранулоцитов. Нет клеток в костном мозге и на периферии. Есть лимфоциты и плазменные клетки. Это характерно для тяжелого агранулоцитоза
-
при миелотоксическом агранулоцитозе - подавление мегакариоцитарного и эритроцитарного ростков, ранние гранулоциты, подавлены. Через 2 недели - нормализация до высокого бластоза ( более 10-20%), часто наблюдается промиелоцитарный костный мозг.
ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ.
-
Если у пациента отмечается некротическая ангина то можно подумать о трех вариантах - острый агранулоцитоз, апластическая анемия, острый малопроцентный лейкоз. В клиническом анализе крови сниженное количество лейкоцитов, относительный лимфоцитоз. При апластической анемии, в отличие от агранулоцитоза, в клиническом анализе крови находят панцитопению. При остром лейкозе наряду с анемией и тромбоцитопенией может быть лейкопения, или лейкоцитоз и бластемия.
-
Инфекционный мононуклеоз. Очень похожа клиника - высокая лихорадка, часто некротическая ангина, но при объективном исследовании можно обнаружить признаки лимфопролиферации, потому что при инфекционном мононуклеозе будет лимфоаденопатия задних шейных узлов, небольшая спленомегалия, гепатомегалия, иктеричность склер.
-
острая лучевая болезнь
-
метастазы в костный мозг
-
пневмония и другие тяжелые инфекции
-
гиперспленизм
-
коллагенозы
-
туберкулез
-
малярия
-
брюшной тиф
-
СПИД
-
семейная нейтропения
ЛЕЧЕНИЕ.
Времени от созревания от стволовой клетки до сегмента требуется 2 недели. Если пациента изолировать (помещение пациента в стерильную боксированную палату) и обеспечить санацию желудочно-кишечного тракта, и держать под контролем возможные очаги вторичной инфекции, с ним ничего не надо делать, он сам выйдет из этого состояния в среднем через 2 недели.
В состоянии агранулоцитоза возможна активизация нормальной флоры кишечника, и генерализация (колисепсис). Санация заключается в назначении неабсорбируемых антибиотиков перорально (это антибиотики которые применяются для парентерального введения - гентамицин, мономиксин, полимиксин). Добавляют микостатики. Все это растворяют в дистиллированной воде и дается перорально.
При количестве лейкоцитов меньше 1 млрд. на л, даже если у пациента нет данных за инфекцию назначают парентерально антибиотики, желательно перекрывающие весь спектр микробной флоры. Оптимально следующее соотношение - цефалоспорины + аминогликозиды + ванкомицин (эффективен против всех штаммов стафилококка). Из цефалоспоринов - фортум до 6 г в сутки, из аминогликозидов - амикацин до 1 г в сутки, ванкомицин - 2 г/сутки. Параллельно обязательно парентерально микостатики, лучшими микостатиком является амфотерицин Б (назначается от 0.5 -1 мг/на кг в сутки).
В настоящее время существуют препараты, которые стимулируют созревание унипотентной стволовой клетки в сторону гранулопоэза (гранулоцитарный колониестимулирующий фактор или Нейпоген, грануломоноцитарный колониестимулирующий фактор - Лейкомакс). Назначая эти препараты можно ускорить выход из агранулоцитоза на 7 дней.
МНОЖЕСТВЕННАЯ МИЕЛОМА.
Это клональное, В-лимфопролиферативное, злокачественное заболевание системы крови, морфологическим субстратом, которого являются плазматические клетки, продуцирующие моноклональные иммуноглобулины. Типичная плазматическая клетка: эксцентрически расположенное ядро; ядро зрелое, с очень конденсированным хроматином, образующим просветления похожие на колесо, встречаются многоядерные клетки; цитоплазма с умеренным просветлением, среди этих клеток встречаются лимфоплазмоцитоидные клетки - очень маленьким размером. Так как клетки содержат большое количество иммуноглобулина А, то клетки при окраске - пламенеющие. Плазматические клетки бывают разной степени зрелости, и это очень важный прогностический фактор при множественной миеломе. Также отмечаются включения в цитоплазму - это скопление молекул иммуноглобулина. Встречаются двуядерные клетки. Специфических морфологических признаков отличающих нормальную плазматическую клетку от опухолевой при миеломе нет. Имеется значение количество - у здорового человека плазматических клеток 1-3.5%, при миеломе 10% и более. То есть важна не морфология, а количество. Количество делящихся клеток очень не велико, при миеломе всего лишь 1% (в здоровом костном мозге количество делящихся клеток от 40 до 50%).
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ. Опухолевая масса является автономной, ее свойственная опухолевая прогрессия. Все этиологические факторы, которые вызывают развитие опухолевого клона клеток, действуют на уровне стволовых, и, как правило, это бывает при миеломе.
Этиологический фактор миеломы не установлен, чаще страдают люди пожилого возраста. Чаще преобладают мужчины, очень низкая заболеваемость в Японии, и очень высокая у негров. Есть данные что ионизирующее излучение может быть этиологическим фактором, но в то же время исследования заболеваемости множественной миеломой населения районов Хиросимы и Нагасаки не выявили увеличения заболеваемости множественной миеломой. Уровень поражения не ясен, но установлено что опухолевый клон уже выявляется на уровне В-клеток. В дебюте заболевания пополнение популяции миеломных клеток происходит за счет популяции В-клеток. В начале заболевания миеломные клетки делятся редко, при рецидиве делятся очень много. Миеломная клетка сама по себе продуцирует очень важный цитокин - интерлейкин-6, и она же содержит рецепторы к этому интерлейкину. Интерлейкин вызывает пролиферацию плазматических клеток, таким образом, миеломы (особенно что касается рецидивирующей миеломы) сами себя стимулируют. Интерлейкин в данном случае выступает в роли аутокринного фактора роста. Этот цитокин продуцируется и стромальными клетками костного мозга, и также стимулирует миеломные клетки и выступает в роли паракринного фактора роста. Интерлейкин ответственен за активность течения заболевания. Также миеломные клетки продуцируют интерлейкин-1-бета, который является составной частью остеокластстимулирующего фактора, остеокласты разрушают кость. Этот интерлейкин стимулирует стромальные клетки к выработки ряда интерлейкинов - интерелейкина-6, интерлейкина-3, грануломоноцитарного колониестимулирующего фактора. Активированные Т-лимфоциты могут продуцировать интерлейкин-4 подавляет пролиферацию миеломных клеток. Интерферон - альфа (вырабатывается у здоровых лиц моноцитами, макрофагами) блокирует рецептор к интерлейкину-6 и таким образом блокирует основное звено патогенеза. Этот препарат (реоферон, интерон А) используется в лечении.
Свойства миеломных клеток такие же, как и у плазматических клеток у здоровых лиц. В норме плазмоциты вырабатывают антитела (иммуноглобулины), эта функция сохраняется у миеломных клеток. Структурно иммуноглобулин, вырабатываемый миеломной клеткой ни чем отличается от нормального иммуноглобулина того же класса (впервые иммуноглобулины были открыты у больных с миеломой). На электрофореграмме распределение иммуноглобулинов, как правило, в сторону какого-либо, в то время как у здорового человека обнаруживается более равномерное распределение иммуноглобулинов. Пик иммуноглобулина объясняется тем что все миеломные клетки идентичны по структуре, и по вырабатываемому иммуноглобулину (G, A, M,E и др.). Выявление такого пика называется выявлением моноклонального белка. Этот белок называется М-градиентом, парапротеином.
Существует метод выявления класса иммуноглобулина - иммунный электрофорез с сыворотками к тяжелым цепям моноклональных белков. Класс моноклонального белка определяется по виду тяжелых цепей (молекула иммуноглобулина состоит из тяжелых и легких цепей).
Классы иммуноглобулинов: A, G, D, E, M. Больше всего среди миелом диагностируется миелома G (53%), миелома А (25%), миелома Д (2%), миелома Е. Считается иммуноглобулин М продуцируется более молодыми клетками - В-лимфоцитами, и для миеломы не характерен.
Бывают биклональные миеломы, когда верифицируются два клона и бывают миелома, которая продуцируется только легкие клетки - при миеломе Бенс-Джонса (болезнь легких цепей). У таких больных моноклональный белок в крови обнаруживаться не будет, уровень общего белка нормальный, но выраженная протеинурия. У таких пациентов уровень протеинурии будет зависеть от величины опухолевой массы и иногда достигает 30-40 г/сут, однако такие пациенты не имеют проявлений нефротического синдрома, потому что протеинурия обусловлена не альбуминами (обеспечивают онкотическое давление).
Очень редко бывают несекретирующие миеломы.
ДИАГНОСТИКА.
-
Обнаружение М-белка (более 35 г/л) в сыворотке и моче.
-
Инфильтрация костного мозга плазматическими клетками (более 30% плазматических клеток в биоптате).
-
Дополнительные клинические признаки, в том числе анемия, остеолитические процессы в костях скелета, поражения почек и гиперкальциемия.
-
Плазмоцитомы в биопсийном материале. Плазмоцитоз костного мозга наблюдают при многих хронических инфекциях и воспалительных процессах в отсутствие М-белка, что затрудняет дифференцировку миеломы с моноклональной гаммапатией неизвестной этиологии.
Для миеломы иногда характерен саркомный тип роста (например прорастание миеломы из ребер в ткань легкого).
Синдромы, возникающие при миеломе:
-
Синдром гипервязкости обусловленные избыточной продукцией иммунноглобулина (монетные столбики, ускоренно СОЭ). Клинически этот синдром проявляется на повышенную утомляемость, слабость, сонливость, у пациентов со стенокардией может провоцироваться ухудшение течения заболевания.
-
Остеодеструктивный синдром. Прежде всего, страдают плоские кости, так как именно там располагаются очаги гемопоэза, где и идет пролиферация опухолевых клеток, а соответственно и стимуляция остеокластов и появление очагов остеодеструкции. Первыми клиническими проявлениями очень часто являются боли в позвоночнике, костях таза, черепе.
-
Почечный синдром. Генез поражения почек при множественной миеломе многопланов. Иммуноглобулины могут откладываться в тканях почек, с нарушением архитектоники почки, начинаются отложения в канальцах. Белковые отложения могут состоять из молекул легких цепей, или превращенные в амилоид. При остеолитическом процессе идет вымывание кальция, который через кровеносное русло выводится почками и при этом идет отложение кальция - кальциноз почек. Инфильтрация почечной ткани может, происходит самими миеломными клетками. Цитокин вызывает пролиферацию мезангиальных клеток клубочка и появляются изменения по типу гломерулонефрита. При редких вариантах миеломы, когда идет высокая выработка интерлейкина 1, когда рано появляются явления ХПН может быть лихорадка (а вообще лихорадка не характерна для миеломы). Генез амилоидоза при миеломе точно такой же, как и при первичном амилоидозе: и там и там существует клон плазматических клеток, которые секретируют легкие цепи, которые фагоцитируются клетками макрофагальной системы разрушаются и из них синтезируются фибриллы амилоида, которые откладываются в тканях. При множественной миеломе клон этих клеток характеризуется всеми свойствами опухолевой прогрессии, при первичном амилоидозе клон не прогрессирует. Часто имеет место амилоидное поражение языка, сердца, суставов, связки.
-
Иммунодефицитный синдром. Только при этом заболевании отмечается угнетение выработки нормальных иммуноглобулинов. Это синдром приводит к частым простудным заболеваниям, и у 90% пациентов наблюдаются восходящие пиелонефриты.
КЛАССИФИКАЦИЯ МИЕЛОМЫ.
-
Миелома 1 стадии: (масса опухоли до 0.6 кг). Гемоглобин не более 100 г/л, иммунноглобулина G не менее 50 г/л, иммуноглобулина А не менее 30 г/л.
-
Миелома 2 стадии (масса опухоли 0.6 - 1.2 кг). Гемоглобин не более 85-100 г/л, иммуноглобулин G не более 50-70 г/л, иммуноглобулин А 30-50 г/л.
-
Миелома 3 стадии (масса опухоли более 1.2 кг). Гиперкальциемия, остелитические процессы. Гемоглобин менее 85, иммуноглобулин G более 7, иммуноглобулин А более 5 г/л.
Клинико-рентгенологическая классификация.
-
Диффузно-очаговые 60% (остеопороз, очаговые поражения костей)
-
очаговая форма 20-30%
-
диффузная форма
-
склерозирующая форма
-
солитарная миелома
-
висцеральные формы
-
первично лейкемическая форма
Существует скрыто протекающая миелома.
Существуют прогностические признаки, которые позволяют в дебюте заболевания прогнозировать вариант течения. Если заболевает мужчина, то чаще злокачественной формой. Если в дебюте заболевания плазматических клеток до 10% , то чаще это активная форма. При агрессивной форме плазмоцитов больше. Для агрессивной формы характерны плазмобласты, зрелые плазмоциты характерны для индолентной формы.
Сывороточный бета-2 микроглобулин - легкая цепь НLА антигена первого класса, которая присутствует на поверхностной мембране клеток. Это микроглобулин выделяется в кровь, если его концентрация в крови более 6 мг/мл то прогноз очень неблагоприятен.
Если имеется сдвиг влево в лейкоцитарной формуле, то это считается очень злокачественная миелома.
studfiles.net
Агранулоцитоз: формы и причины возникновения, признаки, диагностика, как лечить
Автор: Солдатенков Илья Витальевич, врач-терапевт
Агранулоцитоз – гематологическая дисфункция, характеризующаяся снижением в периферической крови особой фракции лейкоцитов — гранулоцитов (среди которых – нейтрофилы, эозинофилы и базофилы). Это клинико-гематологический синдром целого ряда заболеваний, при которых повышается восприимчивость организма к инфекциям. У женщин агранулоцитоз развивается в несколько раз чаще, чем у мужчин. Обычно патологию обнаруживают у лиц старше 40 лет.
Гранулоциты получили свое название благодаря наличию особой зернистости в цитоплазме, обнаруживаемой при окрашивании определенными красителями. Поскольку гранулоциты преобладают в структуре лейкоцитарной формулы, заболевание сопровождается лейкопенией.
Нейтрофилы составляют основу гранулоцитов (более 90%). Это – клетки крови, выполняющие защитную функцию в организме, обеспечивая процесс фагоцитоза и убивая опухолевые клетки. Они поглощают микробы, пораженные клеточные элементы, инородные тела и остатки тканей, вырабатывают лизоцим для борьбы с бактериями и интерферон для инактивации вирусов.
Основными функциями преобладающих нейтрофильных гранулоцитов являются следующие:
- Поддержание иммунитета на оптимальном уровне,
- Активация свертывающей системы крови,
- Обеспечение стерильности крови.
Вырабатываются гранулоциты клетками костного мозга. Особенно интенсивно этот процесс происходит при инфекционном воспалении. Клетки (в первую очередь, нейтрофилы) быстро погибают в очаге воспаления и входят в состав гноя.
В связи с широким применением современных цитостатических средств и проведением лучевой терапии частота случаев патологии значительно возросла. При отсутствии адекватной и своевременной терапии развиваются тяжелые осложнения агранулоцитоза: сепсис, гепатит, медиастинит, перитонит. Летальность при нередко фиксируемой острой форме агранулоцитоза достигает 80 %.
Причины
Агранулоцитоз — серьезная патология, которая не возникает просто так. Причины заболевания весьма существенные и разнообразные.
Эндогенные причины:
- Генетическая предрасположенность,
- Заболевания иммунной системы — коллагенозы, тиреоидит, гломерулонефрит, болезнь Бехтерева, системная красная волчанка,
- Лейкозы, апластическая анемия,
- Метастатическое поражение костного мозга,
- Кахексия.
Экзогенные факторы:
- Вирус Эпштейн-Барра, цитомегаловирусная инфекция, вирусный гепатит, туберкулез,
- Бактериальная инфекция, протекающая в генерализированной форме, сепсис,
- Прием некоторых медикаментов – цитостатиков, бета-лактамных антибиотиков, «Аминазина»,
- Длительная радиотерапия,
- Лучевая нагрузка,
- Воздействие на организм токсических химикатов — бензола, мышьяка, ртути, инсектицидов,
- Химические вещества, входящие в состав косметики, бытовой химии, лакокрасочной продукции,
- Некачественный алкоголь.
Классификация
Агранулоцитоз в зависимости от происхождения бывает врожденным и приобретенным. Врожденная патология является генетически обусловленной и практически не регистрируется.
По клиническому течению агранулоцитоз бывает острым и рецидивирующим или хроническим.
Патогенетическая классификация приобретенной формы патологии:
- Миелотоксический агранулоцитоз или цитостатическая болезнь,
- Иммунный или гаптеновый — с образованием аутоантител в организме человека,
- Идиопатический или генуинный — этиология и патогенез не установлены.
агранулоцитоз в крови (слева) и нарушение продукции клеток в костном мозге (справа)
Иммунный агранулоцитоз
Иммунный агранулоцитоз развивается в результате гибели зрелых гранулоцитов под воздействием антител. В крови обнаруживаются клетки-предшественники нейтрофилов, что указывает на стимуляцию образования этих клеток и подтверждает диагноз. Гибель огромного количества гранулоцитов приводит к отравлению организма и появлению признаков интоксикационного синдрома, которым нередко сопутствует симптоматика основного заболевания.
- Аутоиммунный агранулоцитоз – симптом системных аутоиммунных заболеваний: коллагенозов, склеродермии, васкулитов. В крови образуются антитела к собственным тканям организма. Пусковым механизмом считается наследственная предрасположенность, вирусные инфекции и психологические травмы. Исход и течение аутоиммунного агранулоцитоза определяется особенностями основного заболевания.
- Гаптеновый агранулоцитоз — тяжелая форма патологии, возникающая в ответ на введение определенного медикамента. Гаптены — это химические вещества, приобретающие свои антигенные свойства после взаимодействия с белками гранулоцитов. Антитела прикрепляются к поверхности лейкоцитов, склеивают и разрушают их. Лекарства, часто выступающие в роли гаптенов: «Диакарб», «Амидопирин», «Ацетилсалициловая кислота», «Анальгин», «Индометацин», «Триметоприм», «Пипольфен», «Изониазид», «Эритромицин», «Бутадион», «Норсульфазол», «Фтивазид», «ПАСК». Курсовое прием данных медикаментов приводит к развитию гаптенового или лекарственного агранулоцитоза. Он начинается остро и продолжает развиваться даже после крайне низких доз препаратов.
Миелотоксический агранулоцитоз
Миелотоксический агранулоцитоз — следствие лучевой или цитотоксической терапии, под воздействием которой подавляется рост клеток-предшественников гранулоцитов в костном мозге.
Все гранулоциты имеют общих предшественников – клеток костного мозга (миелобластов)
От дозы ионизирующего излучения и токсичности противоопухолевого препарата зависит тяжесть заболевания. Продукция клеток миелопоэза подавляется также приемом цитостатиков – «Метотрексата», «Циклофосфана», а также некоторых антибиотиков из группы пенициллинов, аминогликозидов, макролидов.
- При миелотоксическом эндогенном агранулоцитозе подавляется образование клеток крови в красном костном мозге опухолевыми токсинами. Постепенно клетки костного мозга замещаются раковыми.
- Экзогенная форма патологии является симптомом тяжелого заболевания, причиной которого является негативное влияние внешних факторов. Клетки костного мозга интенсивно размножаются и обладают высокой чувствительностью к любому отрицательному воздействию окружающей среды.
- Лекарственный тип патологии возникает под воздействием цитостатиков, которые широко применяют в лечении рака и системных заболеваний. Цитостатики подавляют активность иммунной системы и процесс образования гранулоцитов.
Миелотоксический агранулоцитоз часто протекает бессимптомно или проявляется симптомами геморрагического синдрома и некротической энтеропатии:
- Маточными и носовыми кровотечениями,
- Появлением гематом и геморрагий на коже,
- Кровью в моче,
- Схваткообразной болью в животе,
- Рвотой,
- Диареей,
- Урчанием и плеском в животе, метеоризмом,
- Кровью в кале.
Воспаление слизистой кишечника приводит к развитию язвенно-некротической энтеропатии. На оболочке пищеварительного тракта быстро образуются язвы и очаги некроза. В тяжелых случаях развивается угрожающее жизни профузное кишечное кровотечение или появляется клиника острого живота.
Подобные процессы могут протекать на слизистой оболочке мочеполовых органов, легких, печени. Воспаление легких при агранулоцитозе имеет атипичное течение. В легочной ткани образуются крупные абсцессы, развивается гангрена. У больных возникает кашель, одышка, боль в груди.
Отличительными признаками иммунного агранулоцитоза являются:
- Острое начало,
- Лихорадка,
- Бледность кожи,
- Гипергидроз,
- Суставная боль,
- Гингивит, стоматит, фарингит, тонзиллит,
- Гнилостный запах изо рта,
- Гиперсаливация,
- Дисфагия,
- Регионарный лимфаденит,
- Гепатоспленомегалия.
Язвенно-некротические изменения слизистой оболочки полости рта обусловлена ее высокой заселенностью и бесконтрольным размножением сапрофитной микрофлоры. Воспаление глотки, миндалин и десен быстро принимает некротический характер. Под пленками скапливаются и размножаются бактерии. Их токсины и продукты распада быстро проникают в общий кровоток, что проявляется тяжелой интоксикацией, лихорадкой, ознобом, тошнотой и головной болью. Диагноз иммунного агранулоцитоза подтверждают обнаружением антилейкоцитарных антител при серологическом исследовании.
У детей из наследственных форм чаще всего развивается агранулоцитоз Костмана. Носителями измененного гена могут быть как мать, так и отец. У больных изменяется состав крови, нарушается умственное развитие. На фоне полного отсутствия нейтрофилов остается нормальным количество лимфоцитов. Такие дети отстают в физическом и психическом развитии от своих сверстников. Причина мутации гена в настоящее время не установлена. У новорожденных на коже часто появляется гнойные высыпания, на слизистой полости рта — язвы и геморрагии. У детей постарше развиваются отиты, риниты, пневмонии. Эти патологии сопровождаются лихорадкой, лимфаденитом, гепатоспленомегалией.
Заболевание у детей является хроническим. Обострения сопровождаются появлением язв на слизистой оболочке рта и глотки. При повышении гранулоцитов в крови наступает ремиссия. По мере взросления ребенка симптомы постепенно смягчаются.
Осложнениями тяжелых форм агранулоцитоза являются: прободение кишечника, перитонит, воспаление легких, абсцедирование легочной ткани, септическое поражение крови, дыхательная недостаточность, поражение мочеполовой системы, эндотоксический шок.
Диагностика
Диагностика агронулоцитоза преимущественно лабораторная. Специалисты обращают внимает на основные жалобы больных: лихорадку, геморрагии и язвенно-некротических очаги на слизистой.
Диагностические мероприятия, позволяющие обнаружить агранулоцитоз:
- Общеклинический анализ крови – лейкопения, нейтропения, лимфоцитоз, анемия, тромбоцитопения.
- Общеклинический анализ мочи — протеинурия, цилиндрурия.
- Стернальная пункция, миелограмма, иммунограмма.
- Исследование крови на стерильность на пике гипертермии.
- Консультация узких специалистов — ЛОР-врача и врача-стоматолога.
- Рентгенография легких.
Лечение
Лечение больных с агранулоцитозом комплексное, включающее целый ряд мероприятий:
- Госпитализация в гематологическое отделение стационара.
- Помещение больных в боксированную палату, где регулярно проводится обеззараживание воздуха. Полностью стерильные условия помогут предупредить заражение бактериальной или вирусной инфекцией.
- Парентеральное питание показано больным с язвенно-некротической энтеропатией.
- Тщательный уход за полостью рта заключается в частых полосканиях с антисептиками.
- Этиотропная терапия направлена на устранение причинного фактора — прекращение лучевой терапии и введения цитостатиков.
- Антибиотикотерапия назначается больным с гнойной инфекцией и тяжелыми осложнениями. Для этого используют сразу два препарата широкого спектра – «Неомицин», «Полимиксин», «Олететрин». Лечение дополняют противогрибковыми средствами – «Нистатином», «Флюконазолом», «Кетоконазолом».
- Переливание лейкоцитарного концентрата, пересадка костного мозга.
- Применение глюкортикоидов в высоких дозах – «Преднизолона», «Дексаметазона», «Дипроспана».
- Стимуляция лейкопоэза – «Лейкоген», «Пентоксил», «Лейкомакс».
- Дезинтоксикация — парентеральное введение «Гемодеза», раствора глюкозы, изотонического раствора натрия хлорида, раствора «Рингера».
- Коррекция анемии — напр. для ЖДА препараты железа: «Сорбифер дурулес», «Феррум лек».
- Лечение геморрагического синдрома — переливания тромбоцитарной массы, введение «Дицинона», «Аминокапроновой кислоты», «Викасола».
- Обработка полости рта раствором «Леворина», смазывание язвочек облепиховым маслом.
Чтобы предупредить развитие агранулоцитоза, необходимо тщательно контролировать картину крови во время лечения миелотоксическими препаратами, при проведении лучевой терапии и химиотерапии. Таким больным необходимо питаться продуктами, восстанавливающими функции костного мозга. Для этого в рацион следует включать жирные сорта рыбы, куриные яйца, грецкие орехи, куриное мясо, морковь, свеклу, яблоки, свежевыжатые овощные и фруктовые соки, морскую капусту, авокадо, шпинат. С профилактической целью следует принимать витамины, поддерживающие иммунную систему на оптимальном уровне.
Прогноз агранулоцитоза зависит от течения основного заболевания. При развитии септических осложнений он становится неблагоприятным. Заболевание может привести к стойкой утрате трудоспособности и даже смерти больного.
Видео: об агранулоцитозе при химиотерапии
Перейти в раздел:
- Заболевания крови, анализы, лимфатическая система
Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос ответит один из ведущих авторов сайта.
В данный момент на вопросы отвечает: А. Олеся Валерьевна, к.м.н., преподаватель медицинского вузаПоблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
sosudinfo.ru